- Qué es una herida tumoral y por qué es diferente
- Fisiopatología: por qué huele, por qué sangra, por qué duele
- El cambio de objetivo: de curar a cuidar
- Control del olor: lo que funciona y lo que no
- Manejo del exudado: absorber sin traumatizar
- Control del sangrado
- Manejo del dolor en la cura
- Apósitos específicos para heridas tumorales
- El paciente y la familia: lo que no está en el apósito
- Cómo documentar en un contexto paliativo
- Bibliografía
La herida tumoral no se cura. Eso es lo primero que hay que tener claro — y lo más difícil de integrar cuando llevamos años trabajando con el objetivo de cerrar heridas. En la herida neoplásica, el éxito no se mide en centímetros cuadrados de epitelización. Se mide en dignidad, en confort y en calidad de los días que quedan.
Este artículo no trata sobre curación. Trata sobre cómo cuidar una herida que no va a cerrar, con criterio clínico, con honestidad hacia el paciente y con las herramientas correctas para cada problema concreto.
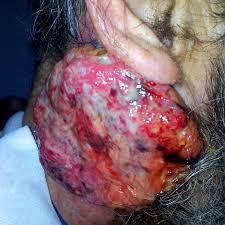
Qué es una herida tumoral y por qué es diferente
Una herida tumoral — también llamada herida neoplásica, fungoide o maligna — es aquella producida por la infiltración de células tumorales en la piel y el tejido subcutáneo, que resulta en una herida abierta que no puede seguir los procesos normales de cicatrización. Puede ser el resultado de un tumor primario que crece hacia la superficie cutánea, de metástasis cutáneas, o de la infiltración directa de ganglios linfáticos o estructuras adyacentes.
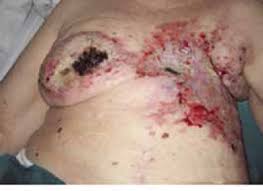
Los tumores que con más frecuencia producen este tipo de heridas en la práctica clínica son el carcinoma de mama (con mucho el más frecuente — hasta el 20% de las pacientes con cáncer de mama avanzado desarrollan afectación cutánea), el carcinoma de cabeza y cuello, el melanoma, el carcinoma de pulmón con extensión torácica y los tumores ginecológicos. También pueden aparecer en cualquier tumor sólido con metástasis cutáneas.
La herida tumoral es diferente a cualquier otra herida crónica en un aspecto fundamental: el agente causal — el tumor — está activo y en expansión. No hay posibilidad de preparación del lecho para la cicatrización mientras el tumor siga creciendo. Los principios del modelo TIME, válidos para la mayoría de heridas crónicas, deben reinterpretarse completamente en este contexto: no estamos preparando el lecho para que cierre — estamos gestionando los síntomas que produce para que el paciente tenga la mejor calidad de vida posible en el tiempo que le queda.
Fisiopatología: por qué huele, por qué sangra, por qué duele
Entender por qué la herida tumoral produce los síntomas que produce es lo que permite elegir la intervención correcta para cada uno de ellos. Los tres síntomas principales — olor, exudado y sangrado — tienen mecanismos distintos y requieren abordajes distintos.
Por qué huele
El olor de la herida tumoral es uno de los síntomas más devastadores para la calidad de vida del paciente y de su entorno. No viene del tumor directamente — viene de la actividad bacteriana sobre el tejido necrótico del lecho. El tejido tumoral mal vascularizado se necrosa de forma continua, creando un sustrato ideal para la proliferación bacteriana anaerobia. Son precisamente las bacterias anaerobias — Bacteroides, Prevotella, Fusobacterium — las que producen los compuestos volátiles responsables del olor fétido característico: putrescina, cadaverina, ácidos grasos de cadena corta.
El olor no indica infección sistémica. Indica colonización de tejido necrótico por flora anaerobia. Esa distinción es importante porque cambia el tratamiento: el objetivo no es esterilizar la herida — es reducir la carga anaerobia lo suficiente para que el olor sea tolerable.
Por qué produce tanto exudado
El exudado abundante de la herida tumoral tiene dos orígenes simultáneos: la hiperpermeabilidad vascular producida por los factores de crecimiento que el tumor secreta (especialmente el VEGF, que aumenta la permeabilidad capilar de forma significativa), y la obstrucción del drenaje linfático local por infiltración tumoral de los ganglios y vasos linfáticos regionales. El resultado es una herida que produce grandes volúmenes de exudado de forma continua que el apósito más absorbente del mercado puede tener dificultades para gestionar.
Por qué sangra
El tejido tumoral tiene una vascularización caótica y frágil — los vasos neoformados del tumor no tienen la estructura normal de los vasos sanos y se rompen ante mínimos traumas. Un apósito adherido al lecho, una maniobra de desbridamiento, incluso la irrigación a presión pueden desencadenar un sangrado que puede ir desde el leve hasta el masivo en heridas muy vascularizadas. El sangrado en heridas tumorales no se gestiona igual que en heridas crónicas convencionales — la fragilidad del tejido hace que muchas medidas habituales sean contraproducentes.
El cambio de objetivo: de curar a cuidar
Control del olor: lo que funciona y lo que no
El olor es el síntoma que más aísla socialmente al paciente y que más impacto tiene en su calidad de vida. Los pacientes con heridas tumorales malolientes frecuentemente dejan de recibir visitas, dejan de salir de casa y desarrollan vergüenza y depresión relacionadas directamente con el olor. Controlarlo no es un objetivo cosmético — es un objetivo terapéutico de primer orden.
Metronidazol tópico — la primera línea
El metronidazol tópico al 0,75–1% es el agente de primera línea para el control del olor en heridas tumorales. Actúa específicamente sobre las bacterias anaerobias responsables de los compuestos volátiles malolientes. Se aplica directamente sobre el lecho de la herida en cada cura. La presentación en gel facilita su aplicación y su permanencia en el lecho. El efecto sobre el olor es generalmente visible en 3–5 días con uso regular.
En algunos centros y comunidades autónomas, el metronidazol tópico puede obtenerse como fórmula magistral o a través de la prescripción oncológica. Vale la pena coordinarse con el equipo de paliativos para tenerlo disponible antes de que el olor sea un problema establecido.
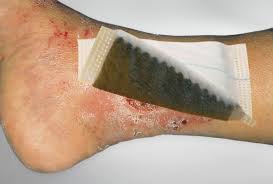
Apósitos de carbón activado
El carbón activado tiene una estructura porosa que adsorbe los compuestos volátiles malolientes antes de que atraviesen el apósito. No elimina el olor en el lecho — lo captura antes de que llegue al exterior. Los apósitos de carbón (Carbonet, Actisorb Silver, Askina Carbosorb) se usan como apósito secundario o único según el nivel de exudado. La limitación principal es que no pueden mojarse — cuando el exudado los satura, pierden su capacidad de adsorción. En heridas muy exudativas, el carbón debe ir como capa exterior sobre un apósito absorbente.
Otras medidas de control del olor
- Irrigación con PHMB o solución de Ringer lactato: la limpieza cuidadosa del lecho en cada cura elimina los restos de tejido necrótico y reduce mecánicamente la carga bacteriana anaerobia. El PHMB tiene actividad antibiofilm y anaerobia adicional. Irrigar a presión baja — no más de 8 psi — para evitar sangrado.
- Desbridamiento del tejido necrótico cuando sea posible y apropiado: eliminar el sustrato que alimenta a los anaerobios es la intervención más eficaz a largo plazo. En heridas tumorales, el desbridamiento cortante es frecuentemente imposible por la fragilidad vascular. El desbridamiento autolítico con hidrogel o hidrofibra puede ser suficiente para el tejido necrótico más superficial.
- Miel de manuka médica: actividad antibacteriana de amplio espectro, incluyendo anaerobios, y capacidad de desbridamiento autolítico leve. Puede ser una alternativa cuando el metronidazol no está disponible o como complemento. Contraindicada en pacientes alérgicos a productos de la abeja.
- Medidas ambientales: ventilar la habitación antes y después de la cura, envolver el apósito retirado inmediatamente, disponer de un contenedor con cierre hermético cerca de la cama. Pequeñas medidas que reducen el impacto del olor en el entorno del paciente.
Manejo del exudado: absorber sin traumatizar
El exudado abundante de la herida tumoral tiene dos consecuencias directas sobre la calidad de vida del paciente: maceración de la piel perilesional cuando desborda el apósito, y necesidad de cambios frecuentes que aumentan el trauma, el dolor y el tiempo dedicado a la cura. El objetivo del manejo del exudado en heridas tumorales no es solo absorber — es absorber suficiente para que el apósito dure el máximo tiempo posible con el mínimo trauma.
- Apósitos superabsorbentes como primera opción en exudado muy abundante: los apósitos superabsorbentes (Zetuvit Plus, Eclypse, DryMax Extra) tienen capacidades de absorción de 500–1000 ml/m² — muy por encima de la espuma o el alginato convencional. En heridas tumorales con exudado masivo, pueden ser la única opción que permita cambios cada 24–48 horas en lugar de varias veces al día.
- Alginato o hidrofibra como relleno de cavidades: cuando hay cavidades o zonas irregulares que producen exudado, el alginato en mecha o la hidrofibra de alta absorción absorben directamente en la fuente antes de que el exudado se extienda. Siempre retirar con humectación previa — nunca a seco en una herida tumoral.
- Protección de la piel perilesional con barrera de forma sistemática: película acrílica o crema con zinc en toda la piel que pueda estar en contacto con el exudado. En heridas tumorales con exudado abundante, la maceración perilesional se desarrolla rápidamente y añade dolor adicional al cuadro.
- Sistemas de recolección para exudado masivo: en heridas con exudado muy abundante — más de 500 ml diarios — los sistemas de bolsa de ostomía adaptada al contorno de la herida pueden ser una opción para el domicilio, permitiendo vaciar sin cambiar el apósito varias veces al día y manteniendo la piel perilesional completamente protegida.
Control del sangrado
El sangrado en heridas tumorales puede ir desde el leve — manchado en el apósito — hasta el masivo y potencialmente fatal en heridas sobre grandes vasos. La prevención es la estrategia principal, porque una vez iniciado el sangrado activo en este tipo de heridas, el manejo puede ser muy difícil.
Prevención del sangrado — técnica atraumática
- Nunca retirar el apósito en seco: humedecer siempre con suero fisiológico antes de retirar, especialmente si hay apósito de gasa o cualquier material que pueda haberse adherido al lecho. Un minuto de humedecimiento puede prevenir un sangrado que requiera 30 minutos de tratamiento.
- Usar siempre apósitos no adherentes como contacto con el lecho: malla de silicona (Mepitel, Urgotul), malla de petrolato, hidrofibra blanda — cualquier material que no se adhiera al tejido friable del tumor. La gasa convencional en contacto directo con la herida tumoral está contraindicada.
- Irrigación a presión baja: la irrigación a presión excesiva puede desencadenar sangrado en el tejido tumoral. Jeringa de 20 ml con palomita — no presión de lavado agresiva.
Manejo del sangrado activo
- Presión directa suave con apósito no adherente: primera medida para sangrado leve-moderado. Mantener durante al menos 10–15 minutos sin levantar para comprobar.
- Alginato hemostático: los apósitos de alginato cálcico tienen efecto hemostático por liberación de iones calcio que activan la cascada de coagulación local. En sangrado leve a moderado, el alginato aplicado directamente sobre la zona sangrante y cubierto con presión suave suele ser suficiente.
- Adrenalina tópica al 1:1000 en gasas: para sangrado activo que no cede con presión. Las gasas empapadas en adrenalina al 1:1000 aplicadas con presión sobre la zona sangrante producen vasoconstricción local. Uso puntual y con vigilancia.
- Protocolo de sangrado masivo — planificación anticipada: en heridas sobre grandes vasos (carótida, subclavia, femoral), la posibilidad de un sangrado masivo debe estar prevista y planificada con el equipo de paliativos y la familia. Las guías de cuidados paliativos recomiendan tener disponibles toallas oscuras (que disminuyen el impacto visual de la sangre), sedación de rescate prescrita de antemano y un protocolo claro sobre qué hacer y a quién llamar. Este protocolo debe establecerse antes de que el sangrado ocurra — no en el momento de la emergencia.
Manejo del dolor en la cura
El dolor durante la cura de una herida tumoral puede ser el más intenso que experimenta el paciente en todo su proceso oncológico. No es exageración — la manipulación de tejido friable, mal vascularizado y con terminaciones nerviosas expuestas produce un dolor que no siempre responde bien a los analgésicos sistémicos que el paciente ya tiene pautados.
- Analgesia previa pautada, no a demanda: administrar el analgésico de rescate 30–60 minutos antes de la cura, de forma sistemática. No esperar a que el paciente refiera dolor durante la cura — a ese punto, el pico analgésico ya ha pasado o todavía no ha llegado.
- Morfina tópica en gel: la aplicación de gel de morfina al 0,1–0,3% directamente sobre el lecho de la herida tiene efecto analgésico local por activación de receptores opioides periféricos. La evidencia es limitada pero la experiencia clínica en unidades de paliativos es favorable para heridas muy dolorosas. Preparación como fórmula magistral.
- Mínima manipulación del lecho: no desbridar lo que no es necesario desbridar. No irrigar más de lo necesario para limpiar. No explorar cavidades innecesariamente. En la herida tumoral, el principio de «primero no dañar» supera al principio de «preparar el lecho».
- Curas lo menos frecuentes posible: el mejor horario de curas es el que produce menos traumas. Si el apósito aguanta 48 horas sin saturarse y sin que haya infección emergente, cambiar cada 48 horas es mejor que cambiar cada 24. Cada cura es un episodio de dolor — reducir las curas es reducir el dolor.
- Entornix (mezcla equimolar de óxido nitroso y oxígeno): donde esté disponible, la analgesia inhalatoria con Entronox durante la cura puede reducir significativamente el dolor procedimental en curas especialmente dolorosas.
Apósitos específicos para heridas tumorales
El paciente y la familia: lo que no está en el apósito
La herida tumoral no es solo un problema de gestión de síntomas. Es una herida que el paciente ve cada día, que le recuerda su enfermedad, que cambia su imagen corporal y que frecuentemente le hace sentir que es una carga para su entorno. El componente psicológico de la herida tumoral es tan clínico como el control del olor o el manejo del exudado — y requiere la misma atención sistemática.
- Nombrar lo que el paciente está viviendo: muchos pacientes no se atreven a hablar del olor, de la vergüenza que les produce tener visitas cuando hay olor, del miedo a que la herida empeore. Preguntar directamente — «¿el olor le está afectando en el día a día?» — abre una conversación que el paciente muchas veces no inicia solo. Como veíamos en el artículo sobre la úlcera terminal de Kennedy, nombrar lo que está ocurriendo con claridad y respeto es parte del cuidado.
- Incluir al paciente en las decisiones del cuidado: preguntarle qué síntoma le molesta más, si prefiere curas más frecuentes o menos frecuentes, si le molesta el olor del material de cura. El paciente con una herida tumoral ha perdido el control sobre muchas cosas — recuperar el control sobre cómo se cuida su herida tiene valor terapéutico real.
- Informar y acompañar a la familia: la familia que cuida a un paciente con herida tumoral también necesita información sobre qué pueden esperar, cómo pueden ayudar y cómo manejar las situaciones difíciles (sangrado, olor intenso, cambio de apósito en domicilio). Una familia que sabe qué puede ocurrir y qué hacer tiene mucha menos ansiedad que una familia que descubre las complicaciones sin preparación.
- No disimular cuando la herida empeora: decirle al paciente que la herida «está mejor» cuando no lo está destruye la confianza en el profesional y le roba al paciente la información que necesita para hacer sus propias elecciones. En el contexto paliativo, la honestidad no es una opción — es parte del respeto.
Cómo documentar en un contexto paliativo
La documentación de una herida tumoral en contexto paliativo tiene un enfoque diferente al de una herida crónica convencional. El objetivo de la documentación no es registrar la evolución hacia la curación — es registrar el impacto de los síntomas en la calidad de vida y la efectividad de las intervenciones sobre esos síntomas.
- Registrar los síntomas, no solo la herida: olor (escala de 0 a 4: 0 ausente, 4 perceptible a distancia), exudado (tipo y cantidad), dolor antes y durante la cura (EVA), sangrado (ausente / leve / moderado / abundante). Esos parámetros son los indicadores de calidad en el manejo paliativo.
- Documentar los objetivos del plan de cuidados: que el plan de cuidados refleje explícitamente que el objetivo es el confort y el control de síntomas — no la cicatrización. Esa documentación protege al profesional y comunica al equipo el marco en el que se están tomando las decisiones.
- Registrar los acuerdos con el paciente y la familia: si el paciente ha expresado preferencias sobre la frecuencia de las curas, sobre qué síntoma prioriza controlar, sobre qué quiere que se haga en caso de sangrado masivo — esos acuerdos deben quedar documentados. La voluntad del paciente en el contexto paliativo tiene el máximo peso clínico y legal.
- Comunicar al equipo médico y de paliativos: cualquier cambio significativo en el patrón de la herida — sangrado que aumenta, olor que empeora a pesar del tratamiento, signos de infección sistémica — debe comunicarse al médico de referencia o al equipo de paliativos. La herida tumoral puede evolucionar rápidamente y requiere un equipo que esté informado.
- 1.Probst S, Arber A, Faithfull S. Malignant fungating wounds: a survey of nurses’ clinical practice in Switzerland. Eur J Oncol Nurs. 2009;13(4):295-298. doi:10.1016/j.ejon.2009.03.008. PMID: 19394264. Prevalencia y manejo clínico de heridas tumorales — encuesta a profesionales de enfermería.
- 2.Alexander SJ. An intense and unforgettable experience: the lived experience of malignant wounds from the perspectives of patients, caregivers and nurses. Int Wound J. 2010;7(6):456-465. doi:10.1111/j.1742-481X.2010.00715.x. PMID: 20849522. Experiencia vivida de pacientes y cuidadores con heridas tumorales — impacto psicológico y calidad de vida.
- 3.Grocott P, Gethin G, Probst S. Malignant wound management in advanced illness: new insights. Curr Opin Support Palliat Care. 2013;7(1):101-105. doi:10.1097/SPC.0b013e32835c0482. PMID: 23360818. Manejo de heridas tumorales en enfermedad avanzada — revisión de evidencia y nuevas perspectivas.
- 4.Schulz V, Triska OH, Tonkin K. Malignant wounds: caregiver-determined clinical problems. J Pain Symptom Manage. 2002;24(6):572-577. doi:10.1016/s0885-3924(02)00542-1. PMID: 12551808. Problemas clínicos determinados por cuidadores — olor, exudado y sangrado como prioridades.
- 5.Gethin G, Grocott P, Probst S, Clarke E. Current practice in the management of wound odour: an international survey. Int J Nurs Stud. 2014;51(6):865-874. doi:10.1016/j.ijnurstu.2013.10.013. PMID: 24268027. Práctica actual en control del olor en heridas — metronidazol y carbón activado como referencias.
- 6.Kalinski C, Schnepf M, Laboy D, et al. Effectiveness of a topical formulation containing metronidazole for wound odor and exudate control. Wounds. 2005;17(4):84-90. Efectividad del metronidazol tópico para el control del olor en heridas tumorales.
- 7.Piggin C, Jones V. Malignant fungating wounds: an analysis of the lived experience. Eur J Palliat Care. 2007;14(3):1-5. Impacto psicológico de las heridas tumorales — análisis fenomenológico de la experiencia del paciente.
- 8.Draper C. The management of malodour and exudate in fungating wounds. Br J Nurs. 2005;14(11):S4-12. doi:10.12968/bjon.2005.14.Sup2.18372. PMID: 16016368. Manejo del olor y el exudado en heridas tumorales — guía práctica.
- 9.Cutting KF, White RJ, Mahoney P. Wound infection, dressings and pain, what is the relationship in the chronic wound? Int Wound J. 2013;10(1):79-86. doi:10.1111/j.1742-481X.2012.00947.x. PMID: 22340423. Relación entre infección, apósitos y dolor en heridas crónicas y tumorales.
- 10.Lo SF, Hayter M, Hu WY, Tai CY, Hsu MY, Li YF. Symptom burden and quality of life in patients with malignant fungating wounds. J Adv Nurs. 2012;68(6):1312-1321. doi:10.1111/j.1365-2648.2011.05839.x. PMID: 22023455. Carga sintomática y calidad de vida en pacientes con heridas tumorales — instrumentos de evaluación y objetivos de cuidado.