- Qué es el hidrocoloide y de qué está hecho
- El mecanismo: cómo forma el gel y por qué eso importa
- El gel amarillo que alarma — y que es completamente normal
- Tipos de hidrocoloide: fino, estándar, anatómico
- Indicaciones: cuándo tiene más sentido que cualquier otro apósito
- Contraindicaciones: cuándo no usarlo por mucho que la herida lo pida
- Marcas disponibles en España y México
- Cómo aplicarlo y cuándo cambiarlo
- Los errores más frecuentes en el turno
- Bibliografía
Hay un apósito que lleva décadas en el mercado, que tiene evidencia sólida para varias indicaciones, que cualquier enfermera conoce de nombre — y que sigue usándose mal con frecuencia. El hidrocoloide.
Se cambia antes de tiempo porque el gel formado «parece pus». Se pone en heridas infectadas porque «algo hay que poner». Se usa en heridas muy exudativas donde se satura en 24 horas y mace
ra los bordes. Y no se usa donde más podría ayudar: en la LPP de categoría I que todavía puede revertirse o en la zona de riesgo que todavía no se ha ulcerado.
El hidrocoloide no es un apósito de relleno. Es un apósito con una biología específica, indicaciones concretas y un comportamiento clínico que hay que saber leer. Este artículo es una revisión completa.
Qué es el hidrocoloide y de qué está hecho
El nombre lo dice todo, si sabemos leerlo: hidro-coloide, un coloide que interacciona con el agua. Los apósitos de hidrocoloide están compuestos por una mezcla de partículas coloidales hidrofílicas — principalmente carboximetilcelulosa sódica (CMC), aunque en diferentes formulaciones se añaden gelatina, pectina y elastómeros — integradas en una matriz de poliisobutileno o poliuretano que actúa como soporte adhesivo.
La CMC es el componente activo esencial. Es un derivado de la celulosa con grupos carboximetilo que le confieren una altísima afinidad por el agua: puede absorber entre 20 y 60 veces su peso en líquido, dependiendo de la formulación y la concentración. Esa capacidad de absorción, combinada con su carácter coloidal, es lo que produce el gel característico del hidrocoloide.
Estructuralmente, la mayoría de hidrocoloides tienen tres capas: una capa interna adhesiva con las partículas coloidales en contacto con el lecho de la herida, una capa intermedia de soporte (espuma de poliuretano en los modelos más modernos) que aporta acolchado y resistencia mecánica, y una capa externa semioclusiva que es impermeable al agua y a las bacterias externas pero permite cierto intercambio de vapor de agua. Esta estructura semipermeable es lo que crea el microambiente húmedo sin producir maceración en la mayoría de indicaciones.
El mecanismo: cómo forma el gel y por qué eso importa
Cuando el hidrocoloide entra en contacto con el exudado de la herida, las partículas de CMC se hidratan y se hinchan absorbiendo el líquido. Al absorber suficiente exudado, las partículas se fusionan entre sí formando un gel coloidal suave, adhesivo y húmedo que permanece en íntimo contacto con el lecho de la herida. Ese gel no es un subproducto — es el agente terapéutico activo del apósito.
¿Qué hace ese gel por la herida? Varias cosas simultáneamente que son el fundamento del principio de cura en ambiente húmedo:
- Mantiene el lecho hidratado: el gel actúa como reservorio de humedad que evita la desecación del tejido en formación. Las células epiteliales migran de 4 a 6 veces más rápido sobre una superficie húmeda que sobre una seca. Este es el fundamento biológico de toda la cura en ambiente húmedo — y el hidrocoloide lo cumple de forma especialmente eficiente porque el gel es semioclusivo pero no completamente oclusivo.
- Favorece el desbridamiento autolítico: el ambiente húmedo creado por el gel activa las enzimas proteolíticas endógenas del propio exudado — colagenasas, elastasas, fibrinolisinas — que van digiriendo el tejido necrótico y el esfacelo blando de forma lenta pero constante. El hidrocoloide es el apósito de desbridamiento autolítico por excelencia cuando hay fibrina blanda o esfacelo y el paciente no puede ser sometido a desbridamiento más agresivo.
- Reduce el dolor en la cura: el gel amortigua la presión mecánica sobre las terminaciones nerviosas del lecho y los bordes, y al mantener el ambiente húmedo evita que las fibras nerviosas queden expuestas al aire en el momento de la retirada. El cambio de hidrocoloide, cuando está bien indicado, es prácticamente indoloro.
- Protege de la contaminación externa: la capa exterior semioclusiva es impermeable al agua y a las bacterias del exterior. Permite ducharse sin cambiar el apósito y reduce el riesgo de contaminación durante las horas entre cambios.
- Reduce la fricción y el cizallamiento: en las LPP en fase de riesgo o categoría I, el hidrocoloide actúa como segunda piel que absorbe las fuerzas de fricción y cizallamiento antes de que lleguen al tejido dérmico. Esta es su indicación preventiva más potente y más infravalorada.
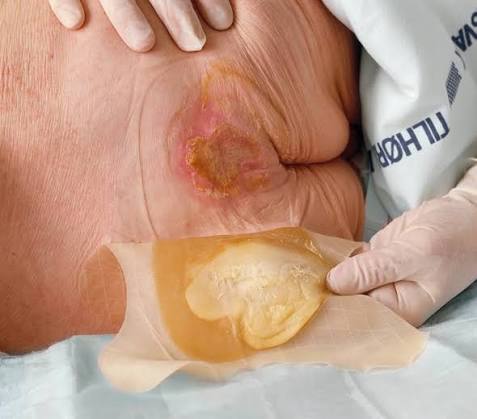
El gel amarillo que alarma — y que es completamente normal
Este punto merece una sección propia porque es el origen del error más frecuente con el hidrocoloide: cambiarlo antes de tiempo por confundir el gel normal con exudado purulento.
Cuando el hidrocoloide lleva 2 o más días en la herida y se retira, lo que aparece debajo es un gel de color amarillo-marrón, ligeramente opaco, con olor característico. Para quien no lo conoce, ese gel tiene un aspecto alarmante — parece pus. Huele mal. Tiene color sospechoso. La primera reacción es pensar que la herida se ha infectado.
Tipos de hidrocoloide: fino, estándar y anatómico
Indicaciones: cuándo el hidrocoloide tiene más sentido que cualquier otro apósito
Más que en cualquier otro apósito, con el hidrocoloide el contexto clínico completo determina si es la elección correcta. No basta con que la herida «sea pequeña» o «tenga poco exudado» — hay que evaluar el estado del lecho, la cantidad de exudado, la presencia o ausencia de infección y la localización.
| Indicación | Tipo recomendado | Por qué |
|---|---|---|
| LPP categoría I — eritema no blanqueable | Fino o anatómico | Protege de fricción y cizallamiento, hidrata la piel, permite monitorizar sin retirar. Puede revertir la LPP I si se actúa pronto. |
| LPP categoría II superficial con exudado mínimo | Estándar | Mantiene el ambiente húmedo, favorece epitelización, protege el lecho del trauma mecánico. |
| Herida con fibrina blanda o esfacelo blando sin posibilidad de desbridamiento cortante | Estándar | El gel activa enzimas endógenas que van digiriendo el tejido no viable. Desbridamiento autolítico lento pero eficaz. |
| Herida en fase de epitelización con exudado mínimo | Fino | Mantiene la humedad necesaria para la migración epitelial sin producir maceración. Permite ver el avance sin retirar. |
| Prevención de LPP en zonas de fricción | Fino o anatómico | Reduce la fricción en zonas de riesgo antes de que aparezca la lesión. Indicación preventiva con evidencia en sacro y talón. |
| Protección de piel perilesional muy frágil o dermatoporótica | Fino | Segunda piel sobre tejido vulnerable que previene el desgarro por fricción con ropa de cama o dispositivos. |
| LPP por dispositivos médicos — fijaciones, sondas, mascarillas | Fino | Bajo el punto de contacto del dispositivo, antes de que aparezca la lesión. Reduce la presión de interface del dispositivo sobre la piel. |
Contraindicaciones: cuándo no usarlo aunque la herida lo pida
El hidrocoloide es un apósito semioclusivo. Esa característica es su mayor ventaja en las indicaciones correctas — y su mayor problema en las incorrectas. Un apósito semioclusivo crea un ambiente anaerobio relativo que puede favorecer el crecimiento bacteriano en heridas que ya tienen carga bacteriana elevada.
- Infección activa con criterios STONEES: el ambiente semioclusivo del hidrocoloide es el opuesto de lo que necesita una herida con infección local activa. Un apósito antimicrobiano — alginato con plata, PHMB, cadexómero yodado — es la elección en ese contexto. Poner un hidrocoloide sobre una herida infectada puede acelerar la progresión de la infección al crear el microambiente ideal para el crecimiento bacteriano anaerobio.
- Exudado moderado-alto: el hidrocoloide estándar tiene capacidad de absorción limitada. En una herida muy exudativa — úlcera venosa activa, herida postdesbridamiento abundante, LPP muy exudativa — se satura en 24–48 horas, el gel desborda los bordes y produce maceración de la piel perilesional. El alginato o la hidrofibra son la elección en ese contexto.
- Necrosis seca o escara dura: el desbridamiento autolítico del hidrocoloide funciona sobre fibrina blanda y esfacelo, no sobre tejido necrótico duro. Una escara seca del talón isquémico no se desbridará con hidrocoloide — y en ese contexto específico, como ya desarrollamos, el desbridamiento está contraindicado. El hidrocoloide sobre necrosis seca no tiene ninguna utilidad.
- Heridas muy profundas o tunelizadas: el hidrocoloide en lámina no puede rellenar cavidades ni tunelizaciones. En esas situaciones, la mecha de alginato o la hidrofibra en cinta son los formatos correctos.
- Piel frágil con adherencia excesiva: en pacientes con dermatoporosis avanzada o con piel muy atrófica, la retirada del hidrocoloide puede producir un desgarro cutáneo. En esos casos, el hidrocoloide de silicona (con adhesivo de silicona en lugar de acrílico) o la protección previa con película barrera son las alternativas. Nunca retirar tirando perpendicularmente — siempre paralelo a la piel y con removedor si es necesario.
Marcas disponibles en España y México: diferencias reales
Cómo aplicarlo y cuándo cambiarlo
La técnica de aplicación del hidrocoloide tiene más impacto del que parece sobre su efectividad y duración. Un apósito mal aplicado se despega antes, no cubre la zona correctamente o produce maceración en los bordes.
- Piel limpia y seca antes de aplicar: limpiar la zona con suero fisiológico y secar bien antes de colocar el apósito. El hidrocoloide adhiere sobre piel seca — si la piel está húmeda por sudoración, exudado o restos del producto de limpieza, el adhesivo no sella correctamente y el apósito se desprende en pocas horas. En la zona perilesional, usar película barrera antes del hidrocoloide si hay exudado que pueda macerar los bordes.
- Margen de 2–3 cm de piel sana alrededor de la herida: el apósito debe cubrir la herida con al menos 2 cm de piel perilesional intacta en todos los bordes. Si el margen es insuficiente, el adhesivo no tiene suficiente superficie de contacto y el apósito se levanta por los bordes antes de tiempo.
- Presionar los bordes con la palma caliente: después de colocar el apósito, presionar con la palma de la mano durante 30–60 segundos. El calor de la mano ablanda el adhesivo y mejora el sellado perimetral — especialmente en los bordes y en zonas con irregularidades cutáneas.
- Cuándo cambiar — criterios clínicos, no calendario: el hidrocoloide se cambia cuando el gel ha alcanzado los bordes del apósito (visible en los modelos transparentes o en los Signal), cuando hay fuga de gel o exudado por debajo de los bordes, cuando hay signos de infección emergente, o cuando el apósito se ha despegado significativamente. En ausencia de estos criterios, puede mantenerse hasta 7 días. Cambiarlo cada 2 días por protocolo fijo es el error más costoso y más frecuente.
- Retirada atraumática: nunca tirar perpendicularmente al plano de la piel. Levantar un extremo del apósito y estirar paralelo a la piel, sujetando la piel perilesional con la otra mano. En pacientes con piel muy frágil, usar removedor de adhesivos en spray o en toallita antes de retirar. El gel formado debajo puede limpiarse con suero fisiológico a presión baja — no frotar.
Los errores más frecuentes en el turno
- Cambiar por el gel amarillo sin evaluar la herida: ya lo desarrollamos — el gel de aspecto turbio y olor es completamente normal. Si los bordes del apósito están secos y la piel perilesional está íntegra, el gel es parte del proceso terapéutico. Retirarlo antes de tiempo destruye el trabajo que el gel estaba haciendo.
- Poner hidrocoloide en heridas infectadas: el ambiente semioclusivo favorece el crecimiento bacteriano en heridas con infección activa. Si hay eritema perilesional en aumento, exudado purulento, dolor en aumento y olor fétido — el hidrocoloide está contraindicado. Las señales de infección local activa son la indicación de un antimicrobiano, no de un semioclusivo.
- Usar hidrocoloide estándar en heridas muy exudativas: el hidrocoloide se satura, el gel desborda los bordes y la piel perilesional se macera. En úlceras venosas con edema activo no controlado, en heridas postdesbridamiento, en LPP muy exudativas — el alginato o la hidrofibra son la elección.
- No dejar margen suficiente: un hidrocoloide que cubre exactamente la herida sin margen de piel sana se despega en horas. El margen mínimo es 2 cm en todos los bordes — más en zonas de movimiento (articulaciones, zona sacra con movilización frecuente).
- Aplicar sobre piel húmeda o con restos de producto: el adhesivo del hidrocoloide no funciona sobre piel húmeda. Secar siempre antes de aplicar — incluyendo los restos de crema hidratante que se hayan aplicado en la piel perilesional. Si la piel tiene algún producto, limpiar con suero antes de colocar el apósito.
- No presionar los bordes tras aplicar: sin el sellado térmico con la palma de la mano, los bordes del hidrocoloide no adhieren correctamente y el apósito se levanta en pocas horas, especialmente en zonas con movimiento o fricción. 60 segundos de presión con la palma tras colocar duplican la duración del apósito en la mayoría de casos.
- 1.Winter GD. Formation of the scab and the rate of epithelialization of superficial wounds in the skin of the young domestic pig. Nature. 1962;193:293-294. doi:10.1038/193293a0. PMID: 14007593. El artículo fundacional del principio de cura en ambiente húmedo — base de todos los apósitos modernos incluyendo el hidrocoloide.
- 2.Dumville JC, Stubbs N, Keogh SJ, Walker RM, Liu Z. Hydrocolloid dressings for healing diabetic foot ulcers. Cochrane Database Syst Rev. 2013;8:CD009099. doi:10.1002/14651858.CD009099.pub2. PMID: 23996006. Revisión Cochrane sobre hidrocoloides en úlceras de pie diabético.
- 3.Heyer K, Augustin M, Protz K, Herberger K, Spehr C, Rustenbach SJ. Effectiveness of advanced versus conventional wound dressings on healing of chronic wounds. J Wound Care. 2013;22(1):1-24. doi:10.12968/jowc.2013.22.1.1. Efectividad comparada de apósitos avanzados incluyendo hidrocoloides en heridas crónicas.
- 4.Santamaria N, Gerdtz M, Sage S, et al. A randomised controlled trial of the effectiveness of soft silicone multi-layered foam dressings in the prevention of sacral and heel pressure ulcers in trauma and critically ill patients. Int Wound J. 2015;12(3):302-308. doi:10.1111/iwj.12wellbeing. PMID: 24684388. Apósitos preventivos en sacro y talón — evidencia comparativa.
- 5.Moore ZEH, Cowman S. Wound cleansing for pressure ulcers. Cochrane Database Syst Rev. 2013;3:CD004983. doi:10.1002/14651858.CD004983.pub3. PMID: 23543529. Limpieza de heridas y mantenimiento del ambiente húmedo en LPP.
- 6.European Pressure Ulcer Advisory Panel, National Pressure Injury Advisory Panel, Pan Pacific Pressure Injury Alliance. Prevención y tratamiento de las lesiones/úlceras por presión. Guía de consulta rápida. EPUAP/NPIAP/PPPIA: 2019. Recomendaciones sobre apósitos preventivos en LPP, incluyendo hidrocoloides anatómicos.
- 7.Bauer JD, Isenring E, Waterhouse M. The effectiveness of a specialised oral nutrition supplement on outcomes in patients with chronic wounds: a pragmatic randomised study. J Hum Nutr Diet. 2013;26(5):452-458. doi:10.1111/jhn.12084. PMID: 23464671. Ambiente húmedo y desbridamiento autolítico — efecto del hidrocoloide sobre el lecho.
- 8.Bouza C, Muñoz A, Amate JM. Efficacy of modern dressings in the treatment of leg ulcers: a systematic review. Wound Repair Regen. 2005;13(3):218-229. doi:10.1111/j.1067-1927.2005.130302.x. PMID: 15953048. Efectividad de apósitos modernos incluyendo hidrocoloides en úlceras de pierna.
- 9.Schultz GS, Sibbald RG, Falanga V, et al. Wound bed preparation: a systematic approach to wound management. Wound Repair Regen. 2003;11 Suppl 1:S1-28. doi:10.1046/j.1524-475X.11.s2.1.x. PMID: 12654015. Modelo TIME — papel del hidrocoloide en el desbridamiento autolítico y mantenimiento del ambiente húmedo.
- 10.Thomas DR, Goode PS, LaMaster K, Tennyson T. Acemannan hydrogel dressing versus saline dressing for pressure ulcers. A randomised, controlled trial. Adv Wound Care. 1998;11(6):273-276. PMID: 10326377. Comparativa de apósitos de mantenimiento del ambiente húmedo en LPP — hidrocoloide entre las opciones evaluadas.