- Por qué este tema merece un post entero
- La fisiopatología que lo explica todo
- El componente isquémico — y por qué el ITB miente
- La infección: de la sospecha a la urgencia
- PEDIS: la clasificación que decide si ingresa o no
- El sondaje con estilete: la prueba que más se infrautiliza
- La descarga: el tratamiento que más se prescribe mal
- La cura local en el pie diabético: principios y errores frecuentes
- La glucemia bloquea la cicatrización más que cualquier apósito la desbloquea
- Cuándo derivar y con qué urgencia
- Lo que ocurre cuando la herida cierra
- Checklist para el turno
Cada 30 segundos se amputa un miembro por complicaciones del pie diabético en algún lugar del mundo. No es una estadística de los noventa. Es de hoy, sostenida en el tiempo, a pesar de décadas de guías, protocolos y formación específica.
Y lo más incómodo de ese dato no es la cifra. Es lo que hay detrás: en la mayoría de esas amputaciones, alguien tuvo delante la herida semanas antes, la vio, la curó, y no derivó a tiempo. No por negligencia. Sino porque el sistema en el que trabajaba — y a veces el conocimiento del que disponía — no estaba preparado para lo que tenía delante.
Este post es largo a propósito. El pie diabético no se entiende a medias.
La mortalidad a 5 años supera el 30% — la de amputación suprapodálica, el 70%. Cifras de oncología de mal pronóstico. Y el pie diabético sigue siendo de las patologías que más tarde se deriva en todo el sistema sanitario.
1. Por qué este tema merece un post entero
La diabetes mellitus afecta a más de 500 millones de personas en el mundo. Entre el 15 y el 25% desarrollará una úlcera en el pie a lo largo de su vida. Y de esas úlceras, entre el 14 y el 20% terminarán en amputación.
El coste no es solo humano. El pie diabético es una de las causas más frecuentes de hospitalización prolongada en pacientes diabéticos, y el coste por episodio es entre 3 y 5 veces superior al de otras úlceras crónicas. Cuando hay amputación, los costes sanitarios directos e indirectos se multiplican exponencialmente — y la calidad de vida del paciente cae de forma brusca e irreversible.
Lo que hace especialmente grave este problema no es su frecuencia, sino su evitabilidad. Se estima que entre el 50 y el 85% de las amputaciones relacionadas con el pie diabético son prevenibles con una detección precoz, un manejo correcto y una derivación a tiempo. Esa es la cifra que debería colgar en cada consulta de enfermería.
2. La fisiopatología que lo explica todo
Para entender el pie diabético hay que entender por qué el paciente no nota lo que le está ocurriendo. Y eso requiere entender las tres neuropatías que actúan antes de que tú veas la herida.
Neuropatía sensorial
Es la más conocida y la que tiene consecuencias más inmediatas. La desmielinización de las fibras sensitivas elimina la percepción del dolor, la temperatura y la presión. El paciente no nota la callosidad que lleva semanas comprimiendo tejido. No nota la ampolla que se rompió con el calzado. No nota que está pisando sobre una zona de presión anormal. Y sigue caminando.
Esto no es incapacidad de cuidado. Es ausencia física de señal. El cerebro no recibe el aviso de que algo está fallando. La exploración de la sensibilidad con el monofilamento de 10 gramos es la prueba de cribado estándar: si el paciente no percibe el monofilamento en los puntos de presión del antepié, tiene neuropatía sensorial establecida y el riesgo de ulceración es 7 veces superior al de la población diabética sin neuropatía.
Neuropatía motora
Menos visible pero igual de relevante. La afectación de las fibras motoras produce un desequilibrio muscular en el pie: los músculos intrínsecos se atrofian, y los extrínsecos compensan de forma anómala. El resultado estructural son los dedos en garra, el antepié prominente, el colapso del arco plantar. Nuevos puntos de presión que antes no existían.
Sobre esos puntos de presión, el paciente —sin la señal de dolor— sigue aplicando la carga corporal con cada paso. El tejido se comprime, la microcirculación se colapsa, se forma la callosidad. Debajo de la callosidad, el tejido necrótico progresa sin que nadie lo vea. Cuando aparece la úlcera, el proceso lleva semanas establecido.
Neuropatía autonómica
La que menos se menciona y la que más subestima el riesgo basal del paciente. La afectación del sistema nervioso autónomo a nivel del pie produce pérdida de la sudoración (anhidrosis), lo que resulta en una piel seca, descamativa, que se agrieta de forma espontánea — especialmente en los talones y en los espacios interdigitales. Sin que el paciente haga nada mal. Sin que lo provoque.
Esas grietas son puertas de entrada directas para la infección. A eso hay que sumar la apertura de shunts arteriovenosos que caracteriza a la neuropatía autonómica: la sangre pasa de arteriola a vénula sin pasar por el capilar. El pie puede tener pulsos palpables y temperatura normal — incluso calor — y sin embargo la microcirculación del tejido estar gravemente comprometida. Es el llamado «pie caliente isquémico» que confunde en la exploración.
3. El componente isquémico — y por qué el ITB miente
La enfermedad arterial periférica (EAP) está presente en el 50-70% de los pacientes con úlcera de pie diabético. Y aquí viene el problema diagnóstico fundamental: el índice tobillo-brazo (ITB) no es fiable en el diabético.
Las arterias tibiales y peroneas en el diabético están sometidas a calcificación de la media (arteriosclerosis de Mönckeberg) que no produce obstrucción pero sí rigidez de la pared arterial. Esas arterias rígidas no se comprimen con el manguito de presión. El resultado: el ITB sale falsamente elevado o «dentro del rango normal» aunque haya isquemia real y el flujo sea insuficiente para sostener la cicatrización.
Un ITB de 1.0 o incluso 1.1 en un pie diabético no garantiza perfusión adecuada. Y un ITB mayor de 1.3 en este contexto no es buena perfusión — es calcificación arterial severa. El número es técnicamente inútil.
Alternativas diagnósticas cuando el ITB no es fiable
La presión sistólica en el dedo del pie (ITB-dedo) es el sustituto más utilizado. Las arterias digitales son menos susceptibles a la calcificación, así que el valor es más fiable. Un ITB-dedo menor de 0.7 indica isquemia significativa. La TcPO2 (presión transcutánea de oxígeno) mide directamente la disponibilidad de oxígeno en el tejido perilesional: por debajo de 30 mmHg el tejido no tiene capacidad de cicatrizar; por encima de 40 mmHg hay margen terapéutico.
Cómo sospechar isquemia en el turno sin pruebas adicionales
No siempre tienes acceso a Doppler o TcPO2. Pero siempre tienes los ojos y las manos. Hay señales que orientan antes de que llegue el resultado de ninguna prueba:
- Lecho pálido o mate en lugar de rojo brillante, con escaso exudado para el tamaño de la herida
- La herida no responde a un tratamiento local que debería funcionar tras 2-3 semanas
- Piel perilesional brillante, fría, con pérdida del vello
- Ulceración en localización atípica: bordes del pie, talón, zonas de compresión del calzado
- Prueba de Buerger positiva: elevación de la pierna a 45° durante 1-2 minutos produce palidez plantar; al bajarla, el tiempo de recuperación del color supera los 15 segundos o aparece rubicundez reactiva intensa
4. La infección: de la sospecha a la urgencia
La mitad de las úlceras de pie diabético se infectan en algún momento de su evolución. Y en las úlceras moderadas o graves, entre el 15 y el 20% terminan en amputación. El diagnóstico precoz de la infección y la correcta gradación de su severidad son las decisiones con más impacto clínico que puedes tomar en el turno.
El problema diagnóstico en el pie diabético es que los signos clásicos de infección están sistemáticamente atenuados. La neuropatía elimina el dolor. La alteración de la respuesta inmune reduce la fiebre, la leucocitosis y la respuesta inflamatoria local. Una herida con infección profunda, afectación de tendones o articulaciones, o incluso osteomielitis establecida puede presentarse con eritema mínimo, temperatura perilesional solo ligeramente elevada, y exudado que no es claramente purulento.
Lo que hay que buscar activamente: calor perilesional desproporcionado, induración, eritema aunque sea discreto, olor de nueva aparición, exudado que cambia de carácter entre curas, herida que no avanza o que retrocede sin explicación aparente, edema que aumenta, glucemia que descontrol sin causa metabólica clara — la glucemia que sube de forma brusca en un diabético bien controlado puede ser el primer signo de infección profunda antes de que haya ninguna señal local evidente.
5. PEDIS: la clasificación que decide si ingresa o no
La clasificación PEDIS (Perfusion, Extent/size, Depth/tissue loss, Infection, Sensation) del IWGDF es el sistema de referencia para la gradación de la infección en el pie diabético. No es burocracia — es lo que te permite comunicarte con el equipo médico con criterio y lo que determina la vía de manejo.
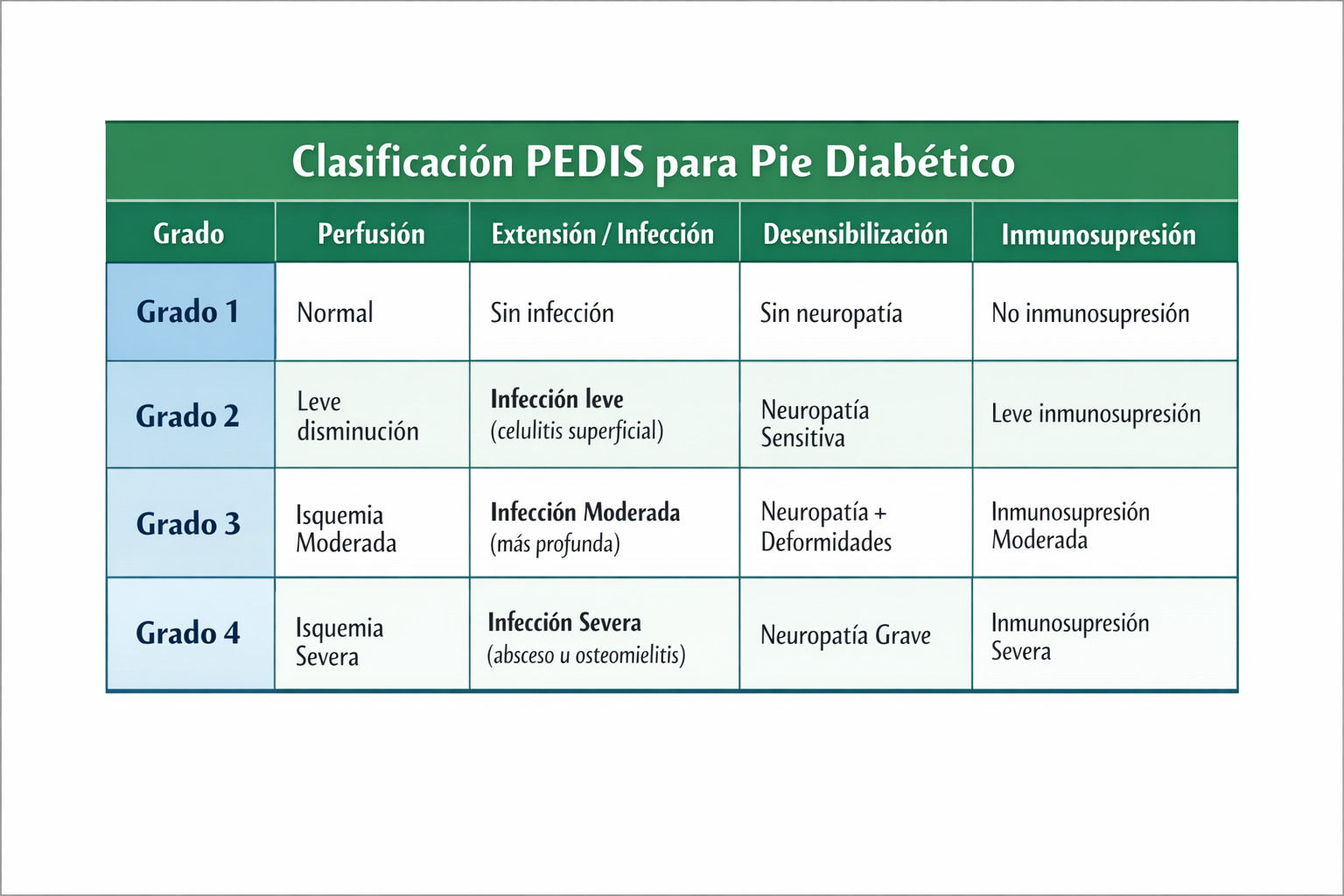
| Grado PEDIS | Criterios clínicos | Manejo |
|---|---|---|
| Grado 1 — Sin infección | Herida sin signos locales ni sistémicos de infección. Lecho limpio, sin calor, sin eritema, sin exudado purulento. | Manejo ambulatorio. Tratamiento local. Seguimiento en consulta. |
| Grado 2 — Leve | Infección local superficial. Eritema ≤2cm perilesional, calor local, induración o exudado purulento. Sin respuesta sistémica. | Ambulatorio. Cultivo (técnica de Levine). Antimicrobial oral según sensibilidad. Revisión a los 5-7 días. |
| Grado 3 — Moderada | Eritema >2cm o afectación de tejidos profundos (fascia, tendón, cápsula articular, hueso), absceso o fascitis. Sin respuesta sistémica. | Valoración urgente hoy. Probable ingreso. Antibiótico IV. Desbridamiento quirúrgico urgente si hay tejido desvitalizado profundo. |
| Grado 4 — Grave | Infección con respuesta sistémica: fiebre >38° o <36°, FC >90, FR >20, leucocitosis o leucopenia, PCR elevada. | Ingreso urgente. Antibiótico IV de amplio espectro. Equipo multidisciplinar. Cirugía vascular si procede. No esperar. |
PEDIS grado 3 o 4 no es manejo de enfermería en solitario ni tampoco puede esperar a la próxima visita programada. Es activar el equipo médico en el día.
6. El sondaje con estilete: la prueba que más se infrautiliza
La osteomielitis en el pie diabético tiene una prevalencia del 20% en las úlceras infectadas, y superior al 60% cuando hay afectación profunda de tejidos. Y el sondaje con estilete metálico estéril tiene una sensibilidad del 89% y una especificidad del 85% para osteomielitis — datos superiores a los de la radiografía simple en estadios precoces.
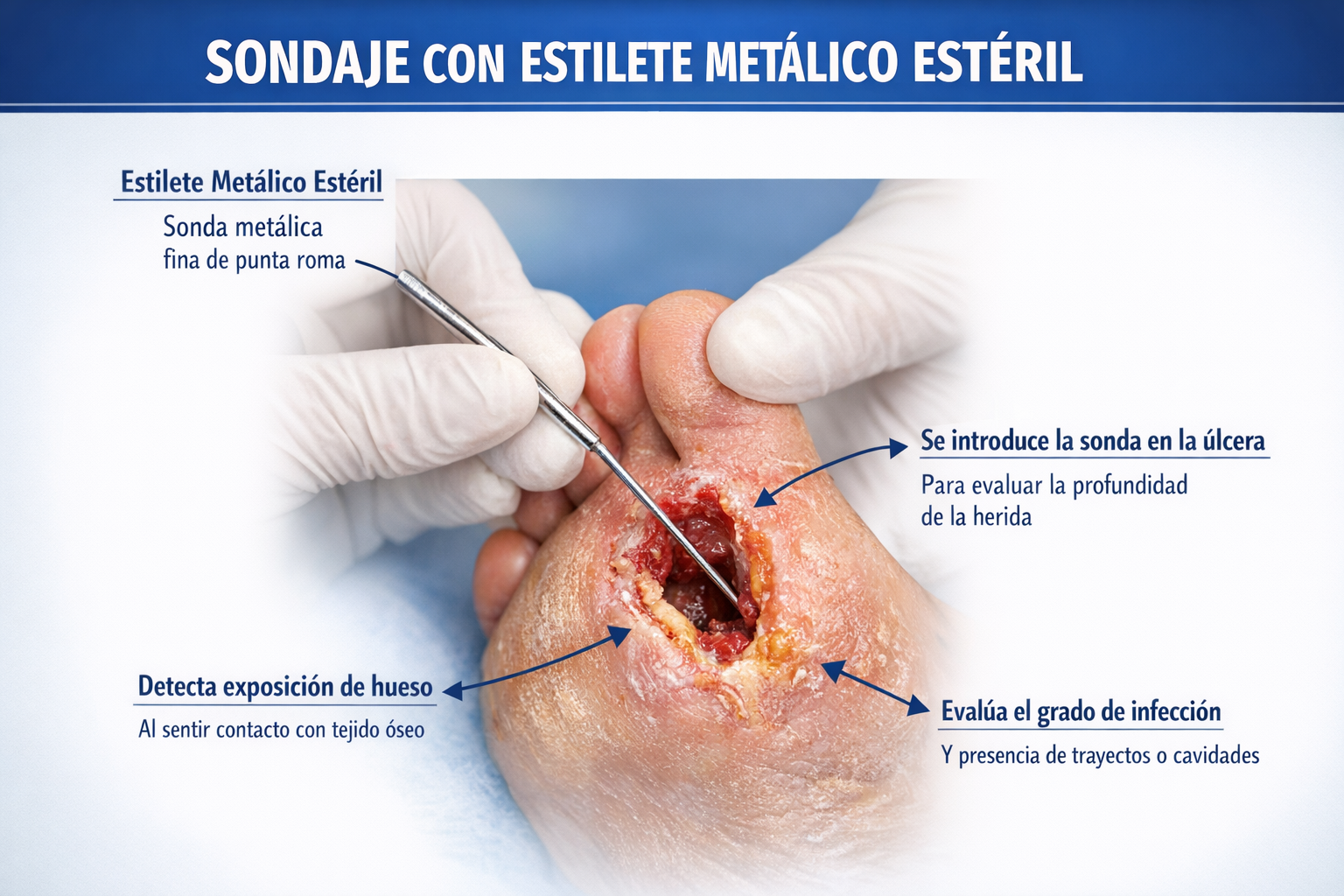
La técnica es sencilla pero requiere hacerla correctamente:
El cultivo: cuándo pedirlo y cómo hacerlo bien
El cultivo de una herida infectada se pide para identificar el microorganismo y conocer la sensibilidad antibiótica — no para confirmar que hay bacterias, porque siempre las hay. Y la técnica importa tanto como la decisión de pedirlo.
Una torunda superficial arrastrada sobre el exudado de la herida cultiva fundamentalmente los contaminantes superficiales, no los microorganismos que están causando la infección en el tejido. El resultado puede ser completamente irrelevante — o, peor, orientar hacia un antibiótico que no va a llegar al foco.
La técnica de Levine es el estándar: tras limpiar la herida con suero para eliminar el exudado superficial, presiona la torunda sobre un centímetro cuadrado de tejido viable — no sobre el esfacelo ni sobre el exudado — y gírala durante cinco segundos con presión suficiente para obtener fluido tisular. Si hay sospecha de osteomielitis, la biopsia ósea es el único cultivo que aporta información diagnóstica real.
7. La descarga: el tratamiento que más se prescribe mal
En las úlceras neuropáticas plantares — las más frecuentes y las que mejor responden al tratamiento cuando este es correcto — la descarga es el tratamiento principal. No el apósito. La descarga.
El yeso de contacto total (TCC) tiene tasas de cierre del 85-90% a las 12 semanas en ensayos clínicos. La bota extraíble, que es lo que se prescribe en la mayoría de los centros por su accesibilidad y porque es más fácil de aplicar, tiene tasas de cierre del 60-65%.
La diferencia no es el dispositivo. Es que la bota se quita. Los estudios con acelerómetros que monitorizan el movimiento real del paciente muestran que la bota extraíble se lleva menos del 30% del tiempo de deambulación. No porque los pacientes sean negligentes — sino porque nadie les ha explicado, con claridad suficiente, que cada paso sin descarga reinicia mecánicamente el daño tisular y anula completamente el efecto de la cura anterior.
Cuando el TCC no es posible — por herida infectada activa, por alteración de la integridad cutánea perilesional, por el perfil del paciente — la alternativa es inmovilizar la bota extraíble con una capa de yeso o fibra de vidrio para hacerla efectivamente no extraíble. La evidencia de esta estrategia — llamada bota no extraíble o «irremovable CAM walker» — es comparable al TCC en varios estudios.
Descarga en la úlcera isquémica o mixta
Aquí las reglas cambian. La descarga sigue siendo necesaria, pero el yeso de contacto total está contraindicado en úlceras con componente isquémico significativo por el riesgo de generar nuevas lesiones por presión en un tejido que no tiene capacidad de respuesta. El manejo requiere descarga adaptada — con revisiones más frecuentes, materiales más amortiguados, y una atención especial a los puntos de prominencia ósea.
8. La cura local en el pie diabético: principios y errores frecuentes
La cura local en el pie diabético no tiene principios distintos a los de cualquier úlcera crónica — TIME, preparación del lecho, equilibrio de humedad, protección perilesional — pero sí tiene varios matices que cambian las decisiones concretas:
El desbridamiento: más cuidado, más criterio
El desbridamiento es necesario cuando hay tejido no viable. Pero en el pie diabético isquémico, la agresividad tiene que calibrarse según el flujo. Con ITB-dedo menor de 0.5 o TcPO2 menor de 30 mmHg, el tejido no tiene recursos para reparar el daño que genera un desbridamiento cortante agresivo. En ese contexto, la escara seca, bien adherida y sin signos de infección se puede proteger en lugar de desbridar, mientras se resuelve el problema vascular.
La escara húmeda, blanda, con eritema perilesional o crepitación — esa sí es urgente, porque indica infección bajo la escara. Ahí sí hay que actuar.
El apósito: secundario al flujo
La elección del apósito en el pie diabético sigue los mismos principios que en cualquier úlcera: adecuarse al nivel de exudado, mantener el equilibrio de humedad, proteger el borde perilesional, minimizar el trauma en el cambio. La malla de silicona como interfase atraumática tiene especial relevancia aquí — la piel perilesional del pie diabético es frágil y el trauma repetido por adhesivos puede generar nuevas lesiones.
Lo que no hay que hacer: usar la elección del apósito como sustituto de las decisiones relevantes. Un apósito de plata no resuelve la isquemia. Un foam no controla el edema si no hay descarga. Y un hidrocoloide no desbridará una fibrina compacta si la herida no tiene flujo para activar la autólisis.
La plata y los antimicrobianos locales: con criterio y tiempo limitado
La plata iónica tiene citotoxicidad sobre fibroblastos y queratinocitos, más pronunciada en tejido hipóxico. En una herida isquémica donde cada célula viable cuenta, usar plata sin indicación clara — o mantenerla durante semanas sin reevaluación — puede frenar la cicatrización que intentas facilitar. El protocolo habitual: 2-4 semanas máximo, con reevaluación a las 2 semanas. Si no hay respuesta clínica, replantear el diagnóstico, no continuar el mismo tratamiento.
9. La glucemia bloquea la cicatrización más que cualquier apósito la desbloquea
Una úlcera de pie diabético con HbA1c por encima del 8% tiene el doble de probabilidad de no cerrar en 12 semanas. Con HbA1c por encima del 10%, el pronóstico es significativamente peor. Es el factor que más frecuentemente bloquea la cicatrización — y el que menos veces se revisa antes de cambiar el apósito.
Los mecanismos son conocidos pero raramente se explican de forma útil en el turno. La hiperglucemia crónica actúa simultáneamente sobre múltiples componentes de la cicatrización:
- Bloquea el cambio del macrófago de perfil M1 (inflamatorio) a perfil M2 (reparador). La herida se queda atrapada en fase inflamatoria de forma indefinida. El tejido se destruye en lugar de reconstruirse.
- Inhibe la síntesis de colágeno por los fibroblastos. Sin colágeno no hay matriz extracelular. Sin matriz no hay granulación estable. Sin granulación no hay cierre.
- Reduce la capacidad bactericida de los neutrófilos. La bacteria que debería eliminarse permanece. La carga bacteriana aumenta. El ciclo inflamatorio se retroalimenta y perpetúa.
- Glicosila las proteínas estructurales del tejido en formación. El tejido cicatricial que se genera tiene menor resistencia mecánica y mayor tendencia a la recidiva.
- Altera la angiogénesis. Sin nuevos vasos, sin oxígeno, sin nutrientes. La granulación no puede avanzar aunque el lecho esté preparado.
Cuando una herida de pie diabético no avanza con un tratamiento que debería funcionar, la primera pregunta no es qué apósito cambio. Es cuándo fue la última analítica, qué ponía la HbA1c y si el equipo médico está al tanto del control glucémico.
10. Cuándo derivar y con qué urgencia
Esta es la decisión que más impacta en el pronóstico — y la que más frecuentemente se retrasa. La regla general: cualquier herida de pie diabético que no mejora en 2-4 semanas con un tratamiento correcto requiere reevaluación diagnóstica y, en la mayoría de los casos, valoración especializada.
Las señales que obligan a actuar hoy — no a esperar la siguiente visita programada:
- Sondaje positivo (contacto óseo con el estilete)
- PEDIS grado 3 o 4 — afectación profunda o respuesta sistémica
- Eritema progresivo que avanza más allá de los 2cm del borde de la herida entre dos curas
- Crepitación perilesional — gas en tejidos blandos hasta que se demuestre lo contrario. Emergencia.
- Descontrol glucémico agudo sin causa metabólica aparente en un paciente previamente estable
- Herida con lecho pálido, exudado escaso y ausencia de respuesta al tratamiento local — sospecha de isquemia crítica
- Necrosis que avanza o que afecta a estructuras profundas
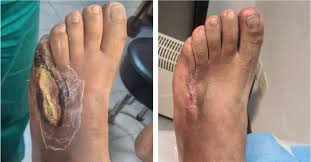
11. Lo que ocurre cuando la herida cierra
El 42% de los pacientes con úlcera de pie diabético que cierra desarrolla otra úlcera en el primer año. No en cinco años. En el primero. El 65% tiene recidiva en los tres primeros años.
El cierre no es el final del tratamiento. Es el inicio de la fase de mantenimiento — que en la mayoría de los sistemas sanitarios no existe de forma estructurada. No hay protocolo de revisión sistemática, no hay seguimiento podológico, no hay control glucémico coordinado post-cierre.
Y el paciente que cerró la herida vuelve a sus zapatos de siempre, con el mismo pie de riesgo que tenía antes — pero ahora con tejido cicatricial menos resistente mecánicamente y reserva vascular más comprometida. Cada recidiva tiene peor pronóstico que la anterior. Y cada amputación parcial modifica la biomecánica del pie de forma que aumenta el riesgo de nuevas úlceras en otras localizaciones.
La mortalidad a 5 años del paciente con úlcera de pie diabético es del 30%. Si ha habido amputación suprapodálica, supera el 70%. Son cifras de oncología de mal pronóstico — y el pie diabético sigue siendo de las patologías que más tarde se deriva en todo el sistema sanitario.
12. Checklist para el turno
Antes de tomar ninguna decisión sobre la cura local, pasa por estas preguntas en orden:
El pie diabético no es una herida difícil de tratar. Es una herida que requiere entender qué hay debajo de lo que se ve. Neuropatía. Isquemia. Infección que no se expresa. Glucemia que bloquea desde dentro. La cura local es el último paso — no el primero.