Los apósitos de colágeno llevan décadas en el mercado de heridas crónicas — el primer producto comercial apareció en 1981 — pero siguen siendo uno de los apósitos más mal indicados en la práctica clínica. Se ponen cuando no hay indicación clara, no se ponen cuando sí la hay, y pocas veces se entiende realmente por qué funcionan en unas heridas y no en otras.
Este artículo explica el mecanismo, revisa la evidencia disponible con honestidad y da las claves clínicas para decidir si un apósito de colágeno tiene sentido en una herida concreta — o si es dinero gastado sin base.
1,53
es el risk ratio de curación con apósito de colágeno frente a cuidado estándar solo, según el metaanálisis de Shu et al. (Frontiers in Surgery, 2022) sobre 11 ECA y 961 pacientes con heridas crónicas. Es decir, el 53% más de probabilidad de curación al añadir colágeno al tratamiento estándar.
1. El colágeno en la cicatrización: de qué hablamos exactamente
El colágeno es la proteína más abundante del cuerpo humano — representa entre el 25 y el 30% del contenido total de proteínas. En la piel, los tipos I y III son los principales componentes estructurales de la dermis. El tipo I forma fibras gruesas que aportan resistencia tensional; el tipo III, más fino y flexible, domina en la fase proliferativa de la cicatrización y es sustituido progresivamente por tipo I durante la remodelación.
En una herida que cicatriza correctamente, el colágeno tiene un papel central en las cuatro fases del proceso:
- Hemostasis: el colágeno extracelular expuesto tras la lesión activa los receptores de las plaquetas (especialmente glucoproteína VI), desencadenando la cascada de coagulación y la formación del coágulo
- Inflamación: los fragmentos de colágeno actúan como señales quimiotácticas que atraen neutrófilos y macrófagos al lecho de la herida
- Proliferación: los fibroblastos producen colágeno tipo III formando la matriz provisional; el colágeno actúa como sustrato para la migración de queratinocitos y la angiogénesis
- Remodelación: el colágeno tipo III es sustituido progresivamente por tipo I, aumentando la resistencia tensional del tejido cicatricial hasta aproximadamente el 80% de la piel original
Los apósitos de colágeno — derivados principalmente de colágeno bovino, porcino o equino de tipo I — se diseñaron para aprovechar estas propiedades y aportarlas directamente al lecho de una herida que no está siendo capaz de generarlas por sí sola.
2. El problema que resuelven: las MMP en las heridas crónicas
Para entender por qué los apósitos de colágeno pueden marcar la diferencia en heridas crónicas — y por qué no funcionan en todas — hay que entender el problema bioquímico que define a una herida crónica estancada.
Las metaloproteasas de matriz (MMP) son enzimas que degradan los componentes de la matriz extracelular. En una herida que cicatriza correctamente, están presentes en concentraciones controladas y su función es necesaria: limpian tejido dañado, facilitan la migración celular y participan en la remodelación. El problema aparece cuando la herida queda atrapada en la fase inflamatoria — que es lo que ocurre en las úlceras crónicas.
En ese estado de inflamación crónica, los niveles de MMP-1, MMP-2, MMP-8 y MMP-9 están marcadamente elevados. Y en esas concentraciones, las MMP no solo degradan tejido no viable — degradan también el colágeno del tejido sano, los factores de crecimiento endógenos (EGF, PDGF, IGF-1) y las proteínas de la matriz en formación. El resultado: tejido de granulación que se destruye antes de consolidarse, factores de crecimiento que se degradan antes de actuar, y un lecho que produce fibrina persistente sin avanzar.

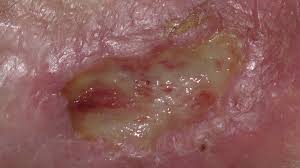
Lecho con fibrina persistente — el exceso de MMP no permite que la matriz en formación progrese. Es el perfil de herida donde el colágeno tiene más sentido
Los apósitos de colágeno actúan principalmente como señuelo competitivo para las MMP. Al proporcionar colágeno exógeno en el lecho de la herida, las MMP en exceso se unen y degradan ese colágeno externo — en lugar de degradar el tejido viable, los factores de crecimiento endógenos y la matriz en formación. Esto es lo que se denomina modulación del entorno proteolítico.
Es importante entender que el colágeno del apósito no va a convertirse en tejido de la herida. Se biodegrada en el lecho. Su función es bioquímica — modificar el entorno — no estructural. Una vez biodegradado, el apósito debe reemplazarse para mantener ese efecto modulador.
3. Cómo actúan los apósitos de colágeno — los 5 mecanismos clave
1
Modulación de MMP — el mecanismo principal
El colágeno tipo I del apósito actúa como sustrato preferente para las MMP-1 en exceso. El colágeno desnaturalizado (gelatina, presente en muchos productos) atrae específicamente MMP-2 y MMP-9. Al secuestrar estas enzimas, protege los factores de crecimiento endógenos y la matriz en formación de su degradación prematura.
2
Matriz provisional para migración celular
El colágeno proporciona un andamiaje tridimensional sobre el que fibroblastos y queratinocitos pueden migrar y proliferar. Las células reconocen el colágeno como sustrato natural a través de receptores específicos (integrinas), lo que facilita su adhesión y migración dirigida hacia el lecho de la herida.
3
Estimulación de fibroblastos
Varios estudios in vitro han demostrado que el colágeno exógeno aumenta la proliferación de fibroblastos y estimula su síntesis de colágeno endógeno. El efecto es especialmente relevante en heridas diabéticas, donde los fibroblastos tienen una actividad intrínsecamente reducida.
4
Mantenimiento del ambiente húmedo
La estructura porosa del colágeno absorbe entre 5 y 7 veces su peso en exudado, formando un gel que mantiene la humedad en el lecho sin macerar el borde perilesional. Este equilibrio es necesario para que las células migratorias funcionen correctamente.
5
Hemostasis y activación plaquetaria
El colágeno es uno de los activadores más potentes de la agregación plaquetaria. En heridas con sangrado activo leve, los apósitos de colágeno tienen efecto hemostático directo — de ahí su uso específico como hemostáticos en cirugía y odontología.

Cutimed Epiona — apósito de colágeno acelular, uno de los más utilizados en la práctica clínica española para heridas crónicas estancadas
Los apósitos de colágeno no son un producto único. Existen en distintos formatos y combinaciones, cada uno con propiedades específicas:
Fuentes del colágeno
La mayoría de los apósitos comerciales usan colágeno bovino o porcino de tipo I, que es bioquímicamente muy similar al humano y tiene baja antigenicidad. Están surgiendo alternativas de colágeno marino (derivado de pescado) y colágeno recombinante humano producido en plantas o levaduras, con potencial ventaja en pacientes con restricciones religiosas o de alergia — aunque estos productos todavía tienen menos evidencia clínica acumulada.
5. Lo que dice la evidencia — con honestidad
Estado de la evidencia — apósitos de colágeno en heridas crónicas
Metaanálisis de 11 ECA (Shu et al., Frontiers in Surgery 2022, n=961): el grupo con colágeno añadido al cuidado estándar tuvo una tasa de curación significativamente mayor (RR=1,53; IC95% 1,33-1,77). Análisis de subgrupos favorable en úlcera diabética, venosa y LPP. Nivel de evidencia GRADE: moderado.
Úlcera de pie diabético — colágeno + ORC (Cirugia Española, ECA): el apósito de colágeno-ORC protegió los factores de crecimiento endógenos (PDGF, EGF, IGF-1) frente a degradación por MMP, con diferencias estadísticamente significativas respecto al grupo control. Reducción de MMP-9 más rápida en el grupo colágeno.
LPP categoría II (revisión sistemática, EPUAP): en estudios con muestra pequeña, tendencia a mayor tasa de cierre con colágeno frente a foam (65% vs 41% de reducción de área, p<0,05 en uno de los estudios más citados). Datos consistentes pero con limitaciones metodológicas.
Úlcera venosa: evidencia más heterogénea. Algunos ECA no muestran diferencias significativas respecto a otros apósitos avanzados cuando la compresión está correctamente aplicada. El colágeno parece aportar más beneficio cuando hay estancamiento a pesar de compresión correcta.
Limitaciones generales: la mayoría de los ECA tienen muestra pequeña (<100 pacientes), definiciones variables de «herida crónica», y escasa uniformidad en la medición de resultados. El nivel de evidencia es moderado — suficiente para apoyar el uso, pero insuficiente para protocolizarlo de forma universal.
La honestidad sobre la evidencia importa aquí: los apósitos de colágeno tienen una base bioquímica sólida y resultados clínicos favorables en la mayoría de los estudios, pero el nivel de evidencia global es moderado — no de grado A. Son una herramienta válida en el arsenal, no una solución universal. Su uso sin criterio clínico claro no tiene base más allá del coste del producto.
6. Cuándo tienen sentido y cuándo no
| ✓ Tiene sentido |
✗ No tiene sentido |
Herida estancada con lecho granulado
Sin avance tras 4-8 semanas con tratamiento correcto. Indicación más sólida. |
Infección activa
Las MMP de la infección degradan el colágeno antes de que actúe. Primero resolver la infección. |
Pie diabético neuropático
Lecho granulado con biocarga controlada. Los fibroblastos diabéticos responden bien al andamiaje externo. |
Herida seca e isquémica
Sin flujo no hay células que aprovechen el andamiaje. La causa vascular va antes. |
LPP categoría II-III
Lecho granulado con progresión lenta. Evidencia favorable aunque con muestra pequeña. |
Causa no resuelta
Si el estancamiento viene de compresión insuficiente, glucemia descontrolada o descarga inadecuada, el colágeno no resuelve nada. |
Post-desbridamiento
Lecho limpio sin granulación activa. El polvo o esponja de colágeno da el andamiaje que necesitan los fibroblastos. |
Lecho con esfacelo extenso
Sin contacto con tejido viable no actúa. Desbridar primero. |
Colágeno + ORC con exudado moderado
La combinación con celulosa oxidada tiene evidencia específica en modulación de MMP. |
Primera línea sin haber probado estándar
Coste muy superior. Reservar para cuando el tratamiento convencional ha fallado. |

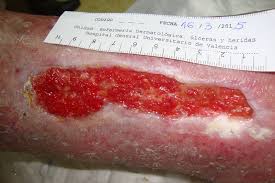
Granulación activa y viable — el lecho donde el colágeno puede actuar como andamiaje para la migración celular. Sin granulación, sin efecto
El apósito de colágeno no sustituye el tratamiento de la causa. En una úlcera venosa, la compresión sigue siendo el pilar del tratamiento — el colágeno es un complemento cuando hay estancamiento a pesar de compresión correcta. En pie diabético, la descarga y el control glucémico van antes. En LPP, el alivio de presión es imprescindible. El colágeno actúa sobre el microentorno del lecho — no sobre las causas sistémicas o mecánicas.
7. Cómo se aplican — protocolo práctico
1
Preparación del lecho
Limpieza con suero fisiológico a presión adecuada. Si hay fibrina o esfacelo, desbridar según el contexto clínico antes de colocar el apósito. El colágeno no desbridará por sí solo un lecho con tejido no viable significativo.
2
Selección del formato correcto
Esponja o lámina para heridas superficiales con exudado moderado. Polvo para heridas cavitadas o irregulares. Colágeno + ORC si el objetivo principal es la modulación de MMP. Colágeno + alginato si el exudado es alto. El formato determina parte del efecto.
3
Aplicación sobre el lecho
Colocar el apósito directamente sobre el tejido viable, cubriendo toda la superficie del lecho. En heridas profundas, puede humedecerse ligeramente con suero antes de aplicar para facilitar el contacto. El contacto íntimo con el tejido es necesario para que actúe.
4
Apósito secundario
El colágeno no es autoadhesivo — siempre requiere apósito secundario. El secundario se elige según el nivel de exudado: foam de baja o media capacidad si el exudado es moderado, film semipermeable si es escaso. El colágeno no debe quedar seco en el lecho.
5
Frecuencia de cambio
Varía según el exudado y el formato. En general, cada 2-7 días dependiendo del nivel de exudado. El colágeno se biodegrada en el lecho — cuando el apósito secundario está saturado o cuando ha pasado el tiempo recomendado por el fabricante, cambia el conjunto. No es necesario retirar fragmentos de colágeno biodegradado si están bien integrados en el lecho.
6
Evaluación a las 2-4 semanas
Si no hay respuesta visible — granulación activa, reducción del área — replantear el diagnóstico antes de continuar. El colágeno no funciona si la causa del estancamiento no es el entorno proteolítico. Biocarga, compresión, descarga y causa sistémica deben estar revisadas.
8. Contraindicaciones y limitaciones reales
| Situación |
Recomendación |
Por qué |
| Infección activa |
Contraindicado |
Las MMP de la infección degradan el colágeno antes de que actúe. Primero resolver la infección. |
| Herida seca e isquémica |
Contraindicado |
Sin flujo no hay células que aprovechen el andamiaje. La causa vascular va antes. |
| Hipersensibilidad al colágeno bovino/porcino |
Contraindicado |
Valorar colágeno de fuente alternativa: marino o recombinante. |
| Exudado muy alto |
Con precaución |
El colágeno puede biodegradarse demasiado rápido. Valorar formato colágeno + alginato o cambios más frecuentes. |
| Lecho con esfacelo extenso |
Con precaución |
Desbridar antes. Sin contacto con tejido viable el efecto es mínimo. |
| Herida que responde al tratamiento estándar |
No indicado |
Coste mayor sin beneficio adicional demostrado. Reservar para cuando el tratamiento convencional ha fallado. |
El coste es un factor real a incluir en la decisión clínica. Los apósitos de colágeno tienen un coste significativamente superior al de los apósitos convencionales. En un sistema con recursos limitados, reservarlos para las heridas donde la evidencia es más sólida — crónicas estancadas con lecho viable, post-desbridamiento, pie diabético con biocarga controlada — es parte del criterio clínico responsable.
Bibliografía
- 1.Shu H, Xia Z, Qin X, Wang X, Lu W, Luo Q, Zhang Z, Xiong X. The clinical efficacy of collagen dressing on chronic wounds: A meta-analysis of 11 randomized controlled trials. Front Surg. 2022;9:978407. doi:10.3389/fsurg.2022.978407. PMID: 36117827.
- 2.Mathew-Steiner SS, Roy S, Sen CK. Collagen in wound healing. Bioengineering (Basel). 2021;8(5):63. doi:10.3390/bioengineering8050063. PMC8235390.
- 3.Khalid S, Mitchell G, Lee K, Rippon MG, et al. Collagen-Based Products in Wound, Skin, and Health Care. Advances in Wound Care. 2025. doi:10.1177/21621918251361118. PMID: 40720447.
- 4.Schönfelder U, Abel M, Wiegand C, Klemm D, Elsner P, Hipler UC. The significance of collagen dressings in wound management: a review. Int Wound J. 2018;15(5):842-851. doi:10.1111/iwj.12942. PMID: 30332361.
- 5.Lantero S, Blanes M, et al. Estudio aleatorizado y comparativo de un apósito de colágeno y celulosa oxidada regenerada en el tratamiento de úlceras neuropáticas de pie diabético. Cirugía Española. 2007;82(1):27-31. doi:10.1016/S0009-739X(07)71629-6.
- 6.Cornwell P. A review of collagen and collagen-based wound dressings. Wounds International. 2009. Flonchi.org — revisión del modo de acción de los apósitos de colágeno. Disponible en: flonchi.org/es/una-revisión-de-colágeno-y-apósitos-para-heridas-a-base-de-colágeno
- 7.Weng YJ, Dong Y, Zhou L, Yang Y, Zhu H. Collagen-Based Wound Dressings: Innovations, Mechanisms, and Clinical Applications. Gels. 2025;11(4):271. doi:10.3390/gels11040271. PMID: 40277707.
- 8.Enfermeriaevidente.com. Uso de apósitos de colágeno en heridas: preguntas y respuestas para enfermería. Noviembre 2025. Disponible en: enfermeriaevidente.com/uso-de-apositos-de-colageno-en-heridas-preguntas-y-respuestas-para-enfermeria
- 9.EPUAP/NPUAP/PPPIA. Prevention and treatment of pressure ulcers/injuries: Clinical practice guideline. European Pressure Ulcer Advisory Panel; 2019. Recomendaciones sobre apósitos avanzados en LPP.
- 10.Kumar M, Banerjee P, Das A, et al. Hydrolyzed collagen powder dressing improves wound inflammation, perfusion, and breaking strength of repaired tissue. Adv Wound Care (New Rochelle). 2024;13(2):70-82. doi:10.1089/wound.2022.0108.
El colágeno no es el apósito milagro que se vende a veces — pero tampoco es marketing vacío. Tiene una base bioquímica real, una indicación específica bien definida y evidencia clínica suficiente para justificar su uso cuando el lecho está bien preparado y la herida sigue sin avanzar. El criterio está en saber cuándo aplica y cuándo no.
— La Dosis Diaria 🩺